
黄海所在鱼类表观基因编辑器及技术体系构建方面取得重要研究进展
发布日期:2026-03-10
浏览次数:10次
DNA甲基化作为表观遗传调控的核心机制之一,通过对基因表达的精准动态调控,深刻影响着生物个体的表型多样性形成,在性别分化、生长发育、抗病抗逆及环境适应等关键生命进程中发挥着不可替代的作用。近年来,基于CRISPR/dCas9的表观基因编辑技术的出现,为实现特定位点的DNA甲基化精准调控开辟了革命性途径。然而,该技术在水生生物尤其是海洋鱼类中的应用仍处于初步探索阶段,面临着编辑器效率不稳定、调控效果难以精准验证、适配海水鱼类复杂生理特性的技术体系不完善等诸多挑战。因此,构建一套更稳定、可重复、易验证的海水鱼类表观基因编辑技术体系,已成为当前水产育种领域突破技术瓶颈、推动种质创新的迫切需求。
依托国家海洋水产种质资源库,中国水产科学研究院黄海水产研究所邵长伟研究员团队以半滑舌鳎和海水青鳉为研究对象,首次在海水鱼类中构建并优化CRISPR/dCas9介导的DNA甲基化编辑技术体系,创建了激活型和抑制型DNA甲基化编辑器,并在技术体系构建和作用机制解析方面取得系列研究进展。相关成果发表于《Zoological Research》《International Journal of Molecular Sciences》等国际学术期刊,并获授权国家发明专利《基于CRISPR/dCas9的适用于半滑舌鳎的DNA甲基化编辑系统及其应用》,实现了从机制研究、技术体系构建到知识产权布局的有机衔接。
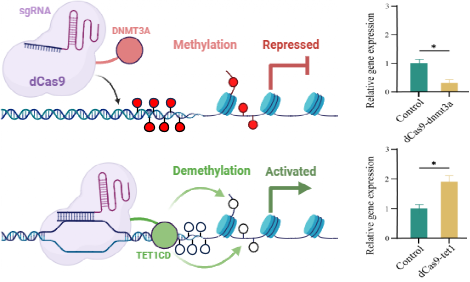
激活型和抑制型DNA甲基化编辑器原理示意图
2024年,研究团队首次在海水鱼类半滑舌鳎中建立了CRISPR/dCas9介导的抑制型DNA甲基化编辑器及技术体系,以生殖发育相关基因emx2为靶标,系统验证了该编辑器在精巢细胞中的可行性。通过靶向提升emx2启动子区域的DNA甲基化水平,显著抑制其转录活性,并引发下游性别分化相关基因的表达改变。编辑效率分析显示,单独转染sgRNA1或sgRNA3时,emx2表达量分别下降约2倍,启动子区甲基化水平分别提高约30%和15.63%;两者联合转染时,emx2表达下调约1.35倍,甲基化水平提高约17.51%。此外,对生物信息学预测的潜在脱靶位点进行检测,未发现脱靶现象。该研究首次在半滑舌鳎中实现了对内源基因甲基化状态的靶向调控,为后续表观遗传编辑体系的拓展与系统优化奠定了技术基础(International Journal of Molecular Sciences, 2024;CN118291539A)。
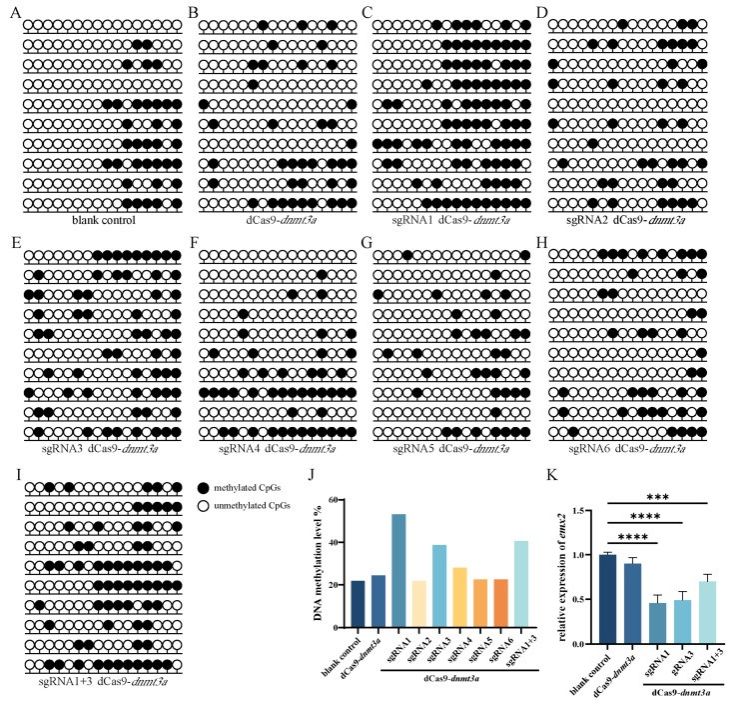
半滑舌鳎emx2基因DNA甲基化编辑
近期,研究团队进一步完善了去甲基化调控方案,并在海水青鳉中构建了更加系统、稳定的CRISPR/dCas9-tet1CD介导的激活型DNA甲基化编辑器及技术体系。以生长调控相关基因fgf2 为研究对象,精确靶向其启动子CpG岛区域,实现高效去甲基化和转录激活。结果显示,该系统可显著激活fgf2的转录活性。其中,Mix1组(sgRNA1+sgRNA2+sgRNA3)和Mix2组(sgRNA2+sgRNA3+sgRNA4+sgRNA5)激活效果最为显著,表达水平分别提升2.18倍和2.41倍,对应启动子区域甲基化水平分别降低22.72%和18.4%,体现出较高的编辑效率与调控精度。全基因组重亚硫酸盐测序和转录组分析进一步表明,该编辑体系未检测到与sgRNA相关的脱靶基因,整体脱靶率极低。值得注意的是,fgf2的表观遗传激活不仅显著增强了其自身表达,还诱导了多种与细胞生长和发育相关下游基因的协同表达变化,并呈现出稳定而持久的调控效应,在dCas9蛋白表达终止9天后仍维持显著上调状态(Zoological Research, 2026)。
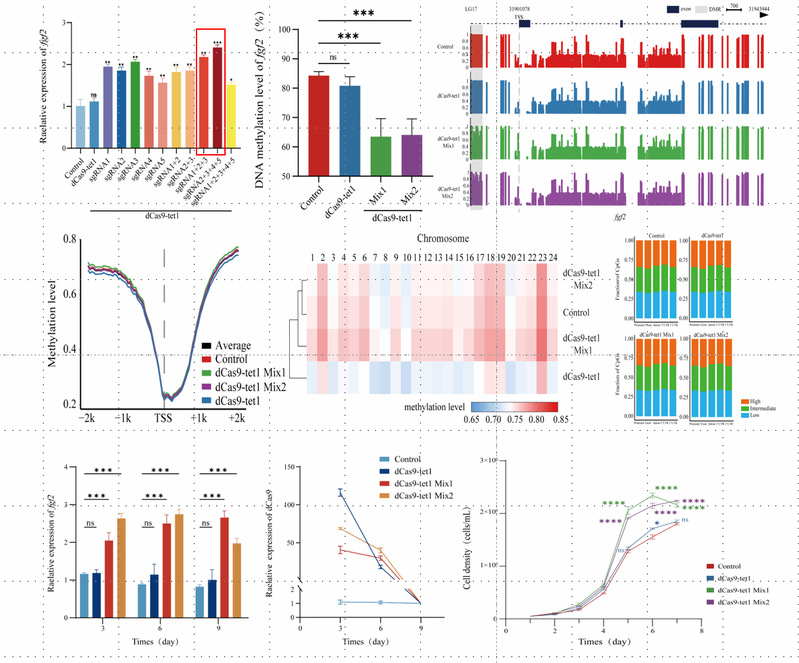
海水青鳉fgf2基因去甲基化编辑
综上,本研究围绕重要海水鱼类功能基因的表观遗传调控,创建了激活型和抑制型2款表观编辑器,建立了一套稳定、可重复、易验证的鱼类表观基因编辑技术体系,揭示了表观遗传可塑性在鱼类生长与发育调控中的重要作用,系统展示了表观编辑技术在鱼类中的应用前景。相关成果从技术路径与分子机制层面深化了对基因调控规律的认识,为功能基因组学研究以及水产种质资源的精准开发与高效利用提供了重要理论基础和技术支撑。
文章链接:
Lin, L., Zhang, J., Liu, B., Du, S., Zhang, Y., Yang, Y., Li, C., Dong, C., He, Y., Wang, Q., et al. (2026). Epigenetic editing of marine medaka (Oryzias melastigma) fgf2 using CRISPR/dCas9-Tet1CD. Zoological Research. 10.24272/j.issn.2095-8137.2025.089
Sun, Y., Wang, H., Liu, B., Yue, B., Liu, Q., Liu, Y., Rosa, I., Doretto, L., Han, S., Lin, L., et al. (2024) CRISPR/dCas9-Mediated DNA Methylation Editing on emx2 in Chinese Tongue Sole (Cynoglossus semilaevis) Testis Cells. International Journal of Molecular Sciences 25, 7637. 10.3390/ijms25147637.
邵长伟, 孙衍旭, 王洪岩, 刘冰花, 岳博文, 刘倩, 刘宇岩, 韩圣磊, 林磊。 基于CRISPR/dCas9的适用于半滑舌鳎的DNA甲基化编辑系统及其应用: 中国, CN118291539A[P]. 2024-07-05.
来源:中国水产科学研究院黄海水产研究所
黄海所在鱼类表观基因编辑器及技术体系构建方面取得重要研究进展
发布日期:2026-03-10
浏览次数:10次
DNA甲基化作为表观遗传调控的核心机制之一,通过对基因表达的精准动态调控,深刻影响着生物个体的表型多样性形成,在性别分化、生长发育、抗病抗逆及环境适应等关键生命进程中发挥着不可替代的作用。近年来,基于CRISPR/dCas9的表观基因编辑技术的出现,为实现特定位点的DNA甲基化精准调控开辟了革命性途径。然而,该技术在水生生物尤其是海洋鱼类中的应用仍处于初步探索阶段,面临着编辑器效率不稳定、调控效果难以精准验证、适配海水鱼类复杂生理特性的技术体系不完善等诸多挑战。因此,构建一套更稳定、可重复、易验证的海水鱼类表观基因编辑技术体系,已成为当前水产育种领域突破技术瓶颈、推动种质创新的迫切需求。
依托国家海洋水产种质资源库,中国水产科学研究院黄海水产研究所邵长伟研究员团队以半滑舌鳎和海水青鳉为研究对象,首次在海水鱼类中构建并优化CRISPR/dCas9介导的DNA甲基化编辑技术体系,创建了激活型和抑制型DNA甲基化编辑器,并在技术体系构建和作用机制解析方面取得系列研究进展。相关成果发表于《Zoological Research》《International Journal of Molecular Sciences》等国际学术期刊,并获授权国家发明专利《基于CRISPR/dCas9的适用于半滑舌鳎的DNA甲基化编辑系统及其应用》,实现了从机制研究、技术体系构建到知识产权布局的有机衔接。

激活型和抑制型DNA甲基化编辑器原理示意图
2024年,研究团队首次在海水鱼类半滑舌鳎中建立了CRISPR/dCas9介导的抑制型DNA甲基化编辑器及技术体系,以生殖发育相关基因emx2为靶标,系统验证了该编辑器在精巢细胞中的可行性。通过靶向提升emx2启动子区域的DNA甲基化水平,显著抑制其转录活性,并引发下游性别分化相关基因的表达改变。编辑效率分析显示,单独转染sgRNA1或sgRNA3时,emx2表达量分别下降约2倍,启动子区甲基化水平分别提高约30%和15.63%;两者联合转染时,emx2表达下调约1.35倍,甲基化水平提高约17.51%。此外,对生物信息学预测的潜在脱靶位点进行检测,未发现脱靶现象。该研究首次在半滑舌鳎中实现了对内源基因甲基化状态的靶向调控,为后续表观遗传编辑体系的拓展与系统优化奠定了技术基础(International Journal of Molecular Sciences, 2024;CN118291539A)。

半滑舌鳎emx2基因DNA甲基化编辑
近期,研究团队进一步完善了去甲基化调控方案,并在海水青鳉中构建了更加系统、稳定的CRISPR/dCas9-tet1CD介导的激活型DNA甲基化编辑器及技术体系。以生长调控相关基因fgf2 为研究对象,精确靶向其启动子CpG岛区域,实现高效去甲基化和转录激活。结果显示,该系统可显著激活fgf2的转录活性。其中,Mix1组(sgRNA1+sgRNA2+sgRNA3)和Mix2组(sgRNA2+sgRNA3+sgRNA4+sgRNA5)激活效果最为显著,表达水平分别提升2.18倍和2.41倍,对应启动子区域甲基化水平分别降低22.72%和18.4%,体现出较高的编辑效率与调控精度。全基因组重亚硫酸盐测序和转录组分析进一步表明,该编辑体系未检测到与sgRNA相关的脱靶基因,整体脱靶率极低。值得注意的是,fgf2的表观遗传激活不仅显著增强了其自身表达,还诱导了多种与细胞生长和发育相关下游基因的协同表达变化,并呈现出稳定而持久的调控效应,在dCas9蛋白表达终止9天后仍维持显著上调状态(Zoological Research, 2026)。

海水青鳉fgf2基因去甲基化编辑
综上,本研究围绕重要海水鱼类功能基因的表观遗传调控,创建了激活型和抑制型2款表观编辑器,建立了一套稳定、可重复、易验证的鱼类表观基因编辑技术体系,揭示了表观遗传可塑性在鱼类生长与发育调控中的重要作用,系统展示了表观编辑技术在鱼类中的应用前景。相关成果从技术路径与分子机制层面深化了对基因调控规律的认识,为功能基因组学研究以及水产种质资源的精准开发与高效利用提供了重要理论基础和技术支撑。
文章链接:
Lin, L., Zhang, J., Liu, B., Du, S., Zhang, Y., Yang, Y., Li, C., Dong, C., He, Y., Wang, Q., et al. (2026). Epigenetic editing of marine medaka (Oryzias melastigma) fgf2 using CRISPR/dCas9-Tet1CD. Zoological Research. 10.24272/j.issn.2095-8137.2025.089
Sun, Y., Wang, H., Liu, B., Yue, B., Liu, Q., Liu, Y., Rosa, I., Doretto, L., Han, S., Lin, L., et al. (2024) CRISPR/dCas9-Mediated DNA Methylation Editing on emx2 in Chinese Tongue Sole (Cynoglossus semilaevis) Testis Cells. International Journal of Molecular Sciences 25, 7637. 10.3390/ijms25147637.
邵长伟, 孙衍旭, 王洪岩, 刘冰花, 岳博文, 刘倩, 刘宇岩, 韩圣磊, 林磊。 基于CRISPR/dCas9的适用于半滑舌鳎的DNA甲基化编辑系统及其应用: 中国, CN118291539A[P]. 2024-07-05.
来源:中国水产科学研究院黄海水产研究所